
Reakcje alkilowania fenyloacetylenu
Larcheveque27 przeprowadził reakcję alkilowania fenyloacetylenu jodometanem oraz bromobutanem. Reakcja była prowadzona w obecności sproszkowanego litu w mieszaninie heksametylofosforotriamidu (HMPT) i benzenu. Do tej mieszaniny dodano fenyloacetylen, a następnie roztwór jodometanu w Et2O lub 1-bromobutan w tetrahydrofuranie (THF). Reakcje prowadzone były w temp. wrzenia mieszaniny. Otrzymano 1-fenylopropyn z wydajnością 60%, a 1-fenyloheksyn, 73%.


Wykorzystując pochodną magnezoorganiczną przeprowadzono alkilowanie fenyloacetylenu t-bromobutanem w Et2O. Do mieszaniny zawierającej bromek etylomagnezowy rozpuszczony w Et2O i schłodzony do temp. 0°C dodano fenyloacetylen i całość ogrzewano i mieszano. Dodano t-bromobutan w schłodzonym Et2O i reakcję prowadzono w temp. wrzenia rozpuszczalnika przez 20 godz. Wydajność 1-fenylo-3,3-dimetylobutynu wynosiła 50%.28
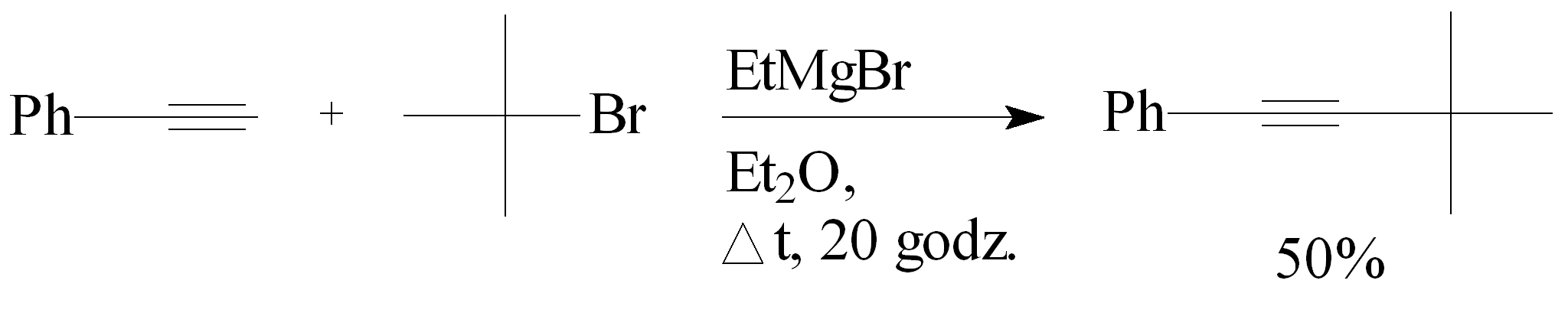
Reakcję jodometanu z fenyloacetylenem przeprowadzono w układzie stały KOH - DMSO
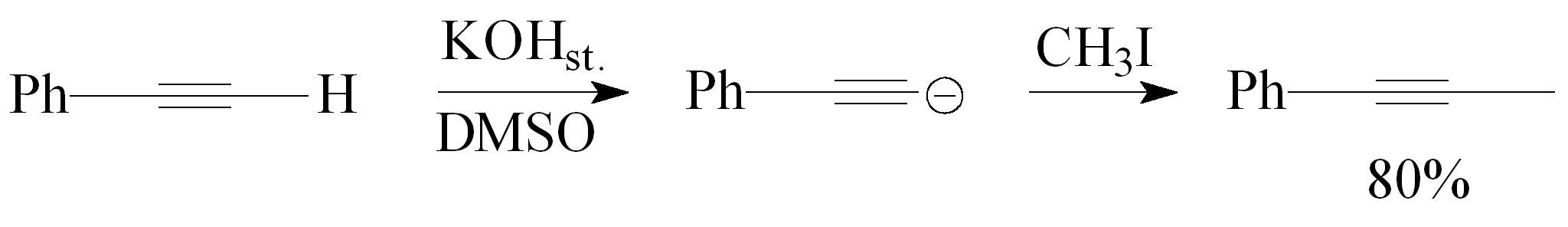
Użyto 2-krotny molowy nadmiar jodometanu oraz 3-krotny nadmiar KOHst. względem alkinu. Reakcję mieszano w temp. 18ºC przez 1.5 godz., a pochodną fenyloacetylenu otrzymano z wydajnością 80%.29
Ponadto przeprowadzono tę reakcję bez użycia czynnika alkilującego i otrzymano trans-1,4-difenylobuten-3-yn z wydajnością 70%.29
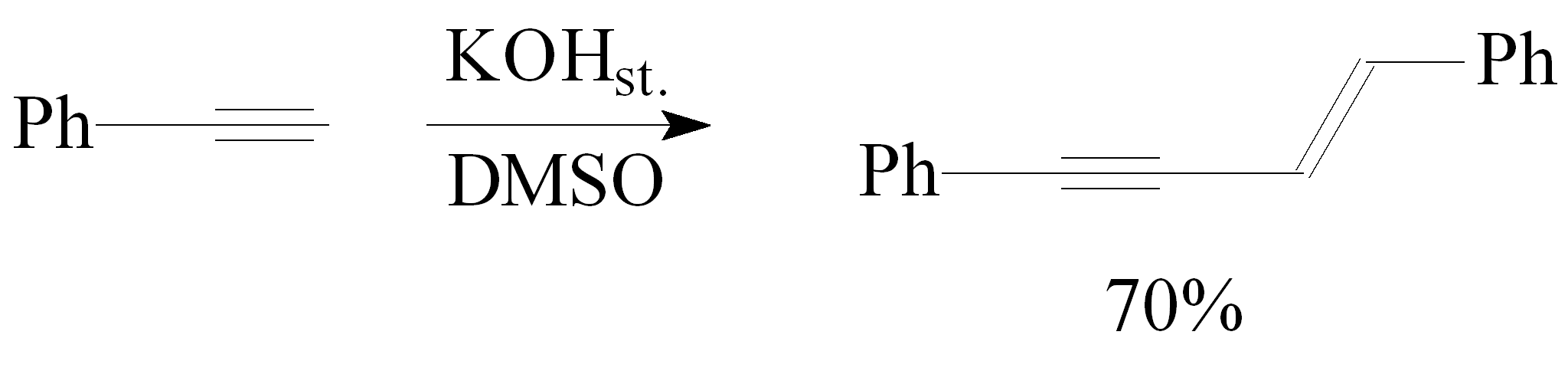
Alkilowanie fenyloacetylenu 1-bromo-3-metylobuta-1,2-dienem przeprowadzono w obecności dietyloaminy, katalizatora palladowego Pd[P(Ph)3]4 oraz kokatalizatora CuI. Reakcję prowadzono w atmosferze argonu, w temp. pokojowej przez 3 godz. Otrzymano produkt z wydajnością 78%.30
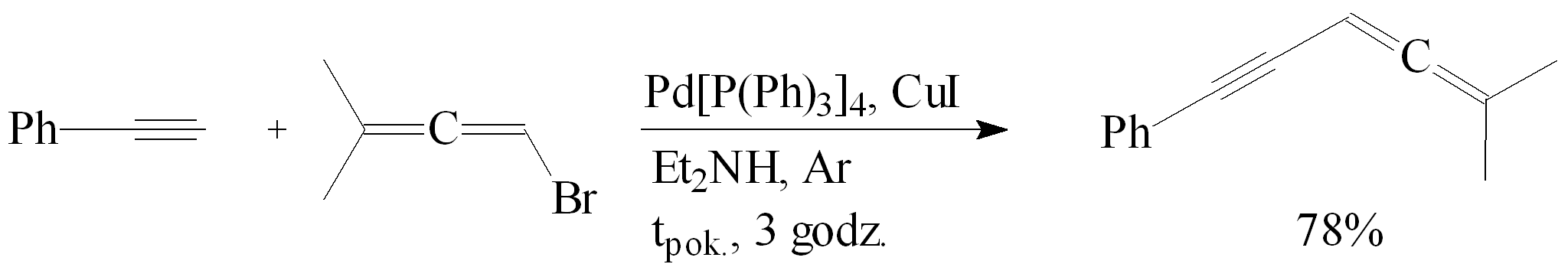
Chong i Wong31 przeprowadzili alkilowanie fenyloacetylenu 1-bromodekanem w obecności kompleksu MeLi·LiBr2. Do fenyloacetylenu rozpuszczonego w THF dodano MeLi·LiBr2 rozpuszczony w ochłodzonym Et2O. Mieszaninę reakcyjną schłodzono do 0°C i mieszano przez 15 min., następnie dodano 1-bromodekan w DMSO, całość mieszano w temp. pokojowej przez 3 godz. Wydajność 1-fenylododekynu wynosiła 85%.
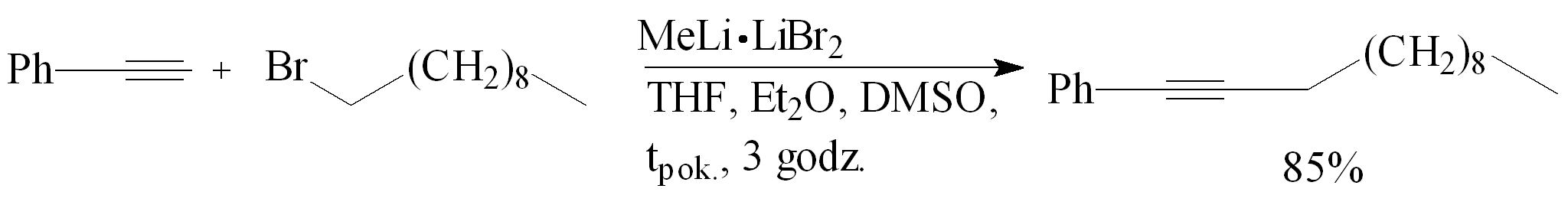
Reakcję alkilowania fenyloacetylenu jodometanem przeprowadzono naświetlając mieszaninę ultradźwiękami. Zawiesinę litu w oleju mineralnym umieszczono w atmosferze suchego azotu, dodano THF, fenyloacetylen i mieszaninę poddano działaniu ultradźwięków (50-60Hz) przez 5 min. Następnie mieszaninę schłodzono do -78°C, dodano jodometan i całość mieszano w temp. pokojowej przez 30 min. Wydajność 1-fenylopropynu wynosiła 95%.32

W 1987 opublikowano wyniki badań alkilowania fenyloacetylenu halogenkami allilowymi w obecności K2CO3 i katalizatora CuI oraz NaI w DMSO. Reakcję prowadzono w atmosferze argonu w temp. 20-45ºC w czasie od 40 do 100 min.33
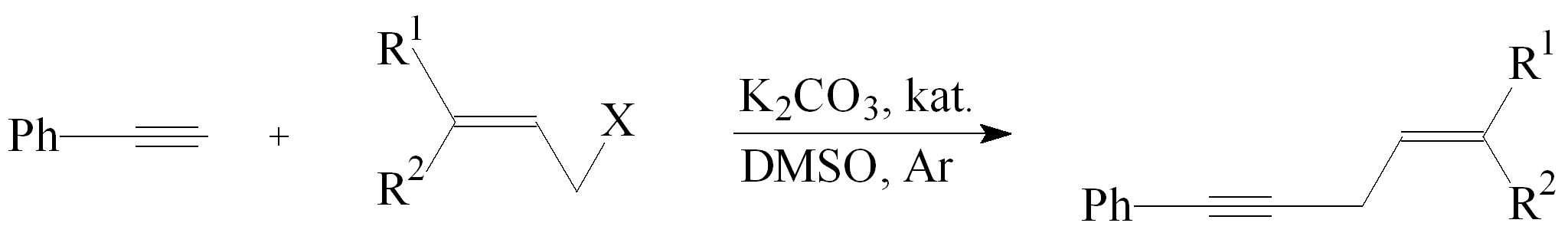
Wyniki reakcji przedstawiłem w Tabeli 1.
Tabela 1
| R1 | R2 | X | Kat. | Temp. [°C] | Czas [min.] | Wydajność [%] |
| H | H | Br | CuI | 20 | 40 | 83 |
| CH3 | CH3 | Cl | CuI | 40 | 80 | 94 |
| CH3 | Cl | Cl | CuI-NaI | 45 | 100 | 92 |
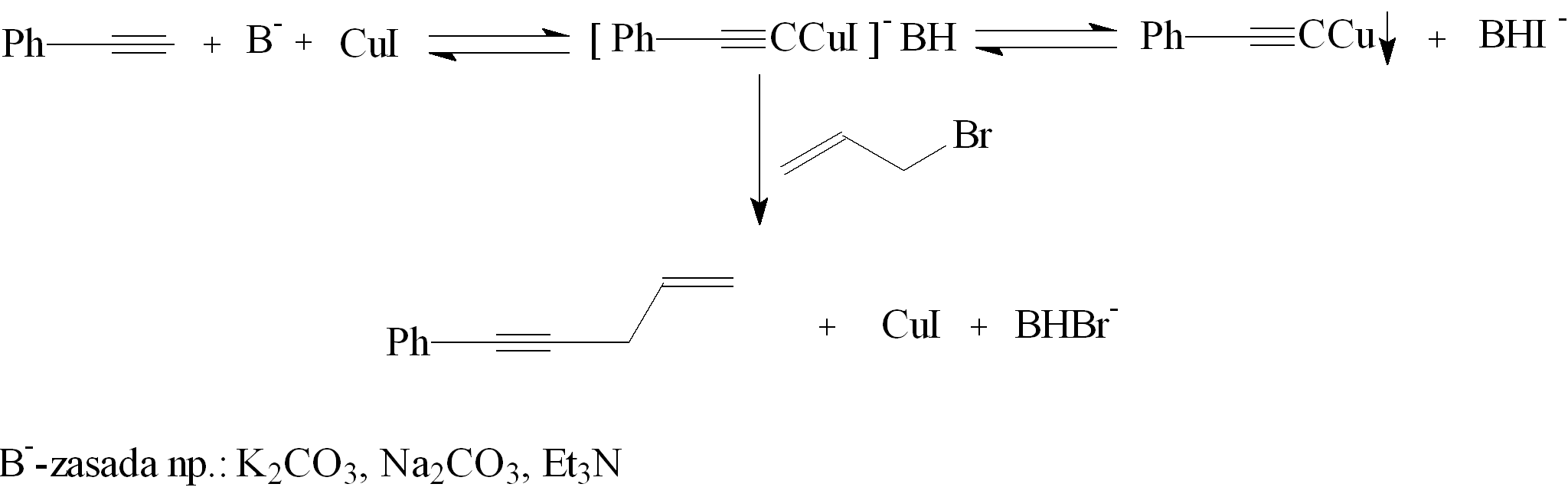
Autorzy przedstawili również mechanizm tej reakcji.
Wykorzystując CuI oraz HMPT przeprowadzono reakcje fenyloacetylenu z podstawionymi halogenkami winylowymi. Reakcje prowadzono w atmosferze azotu w temp. 120°C przez 12-104 godz. (Tabela 2).34
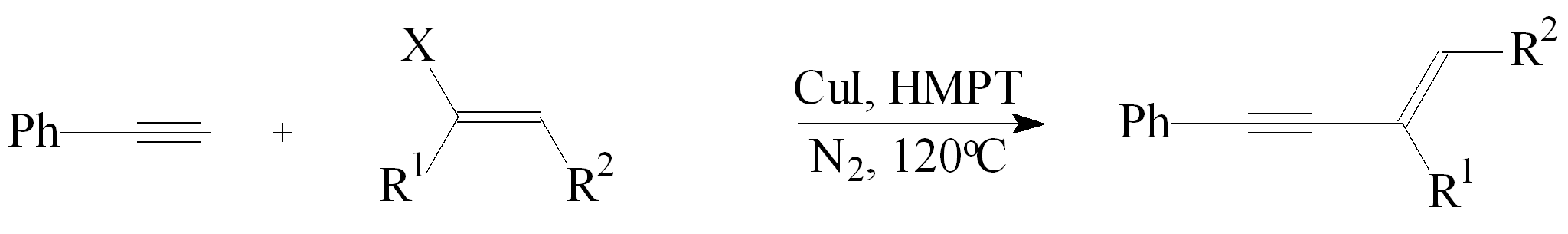
Tabela 2
| R1 | R2 | X | Czas [godz.] | Wydajność [%] |
| H | C6H13 | I | 104 | 87 |
| H | Ph | I | 29 | 43 |
| PhCH2 | H | Br | 12 | 52 |
Wykorzystując układ t-BuOK-DMSO przeprowadzono reakcję alkilowania fenyloacetylenu jodometanem. Jodometan użyto w 4-krotnym molowym nadmiarze, a zasadę w 3-krotnym molowym nadmiarze w stosunku do fenyloacetylenu. Do fenyloacetylenu rozpuszczonego w suchym DMSO dodano t-BuOK i mieszano w atmosferze azotu w temp. 15°C przez 3 godz. Zauważono efekt termiczny reakcji. Otrzymano 1-fenylopropyn z wydajnością 64%.35
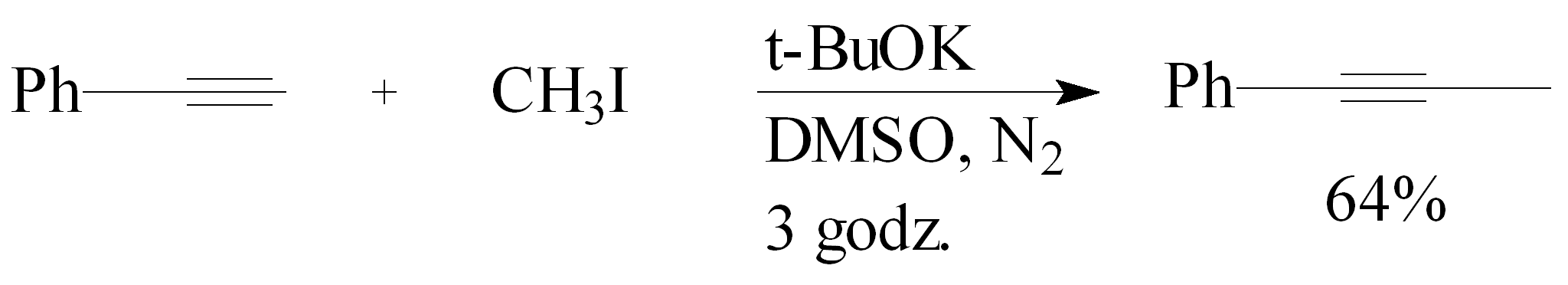
Przeprowadzono reakcję alkilowania fenyloacetylenu halogenkami arylowymi i winylowymi. W roli katalizatora wykorzystano PPh3 oraz jako kokatalizator CuI, zasadą był K2CO3, a rozpuszczalnikiem N,N-dimetyloformamid (DMF). Składniki reakcji były mieszane atmosferze azotu w temp. 120°C (Tabela 3).36,37
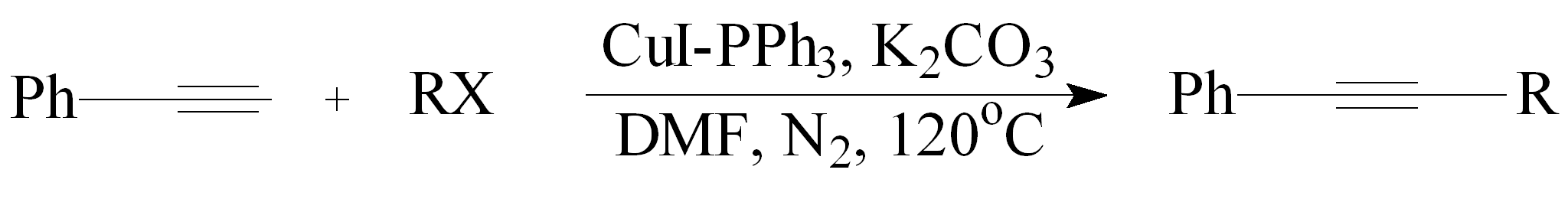
Tabela 3
| RX | Czas [godz.] | Wydajność [%] |
| n-C6H13CH=CHI | 10 | 96a |
| PhCH=CHBr | 24 | 88 |
| PhBr | 48 | 8 |
| PhI | 16 | 98 |
| 1-I-naftalen | 24 | 84 |
| 2-I-naftalen | 17 | 92 |
| 4-NO2C6H4Br | 22 | 5 |
| 2-NO2C6H4Br | 24 | 23b |
| 4-CH3C6H4I | 24 | 95 |
| 4-ClC6H4I | 24 | 92 |
| 4-NO2C6H4I | 16 | 95 |
| 2-CH3OC6H4I | 18 | 84 |
| 2-CH3O2CC6H4I | 24 | 42 |
| 2-CH3O2CC6H4I | 24 | 70c |
| 2-NH2C6H4I | 41 | 78 |
| PhCH=CHI | 28 | 72a |
| Ph(CH3)C=CHI | 20 | 93 |
| n-C5H11CH=CHI | 5 | 92 |
| i-C3H7CH=CHI | 14 | 78 |
a) reakcja prowadzona w temp. 80°C
b) reakcję prowadzono w DMSO
c) dodano H2O równomolowo względem RX
Badając reakcję fenyloacetylenu z jodobenzenem wobec K2CO3 w DMF, którą prowadzono w temp. 120ºC przez 5 godz. Określano zależność wydajności od użytego katalizatora fosfoniowego, jego stosunku względem CuI (Tabela 4), a także od rodzaju użytej soli miedzi (Tabela 5).37
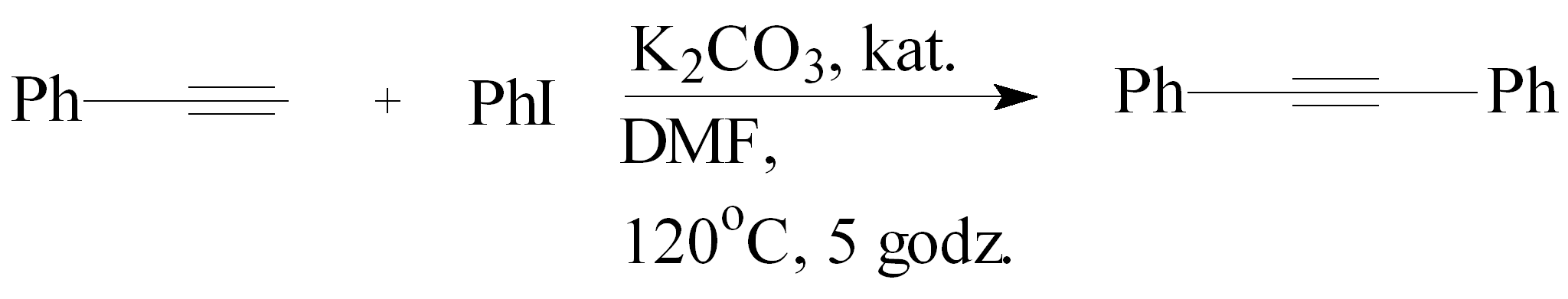
Tabela 4a
| Katalizator | Kat. / CuI | Wydajność 14a [%] | Nieprzereagowany jodobenzen [%] |
| -- | -- | 6 | 91 |
| PPh3 | 1.0 | 40 | 54 |
| PPh3 | 2.0 | 50 | 44 |
| PPh3 | 3.0 | 25 | 70 |
| PPh3 | 4.0 | 21 | 77 |
| PPh3 | 2.0 | 7 | 72 |
| n-BuPPh2 | 2.0 | 12 | 80 |
| n-Bu3P | 2.0 | ilości śladowe | 95 |
| P(OPh)3 | 2.0 | 6 | 91 |
a) warunki reakcji: jodobenzen (2.0 mmol), fenyloacetylen (2.0 mmol), CuI (0.1 mmol), K2CO3 (3.0 mmol),
DMF, 120°C, 5 godz.
Tabela 5a
| Ko-katalizator | Czas [godz.] | Wydajność [%] | Nieprzereagowany jodobenzen [%] |
| CuI | 16 | 98 | 0 |
| CuI | 12 | 99b | 0 |
| CuBr | 16 | 95 | 3 |
| CuCl | 20 | 98 | 1 |
| Cu2O | 20 | 7 | 91 |
| CuCl2 | 20 | 7 | 90 |
| Cu(OAc)2 | 20 | 88 | 5 |
a) warunki reakcji: jodobenzen (2.0 mmol), fenyloacetylen (2.0 mmol), PPh3 (0.2 mmol), K2CO3 (3.0 mmol),
DMF, 120°C, 5 godz.
b) reakcja prowadzona w DMSO
Na podstawie przeprowadzonych badań autorzy przedstawili możliwy mechanizm reakcji katalitycznego alkilowania alkinu halogenkami arylowymi. Reakcja biegnie poprzez kompleks miedzi z obojętnymi ligandami (PPh3, rozpuszczalnik), który ulega dalszym przekształceniom.

Opisano katalityczne alkilowanie fenyloacetylenu 1-jodohept-1-enem wobec Pd[P(Ph)3]4. Syntezę przeprowadzono w pirolidynie w temp. 25°C w ciągu 10 min. Otrzymano 1-fenylonon-3-en-1-yn z wydajnością 95%.38

Reakcję alkilowania fenyloacetylenu przeprowadzono bromkiem allilu wobec odczynnika Grignarda i CuI. Fenyloacetylen rozpuszczony w THF ochłodzono do temp. 0°C i dodano związek magnezoorganiczny w Et2O, a następnie CuI. Do roztworu dodawano podczas mieszania bromek allilu. Reakcja trwała 6 godz., a wydajność otrzymanego 5-fenylopenten-4-ynu wynosiła 70%.39
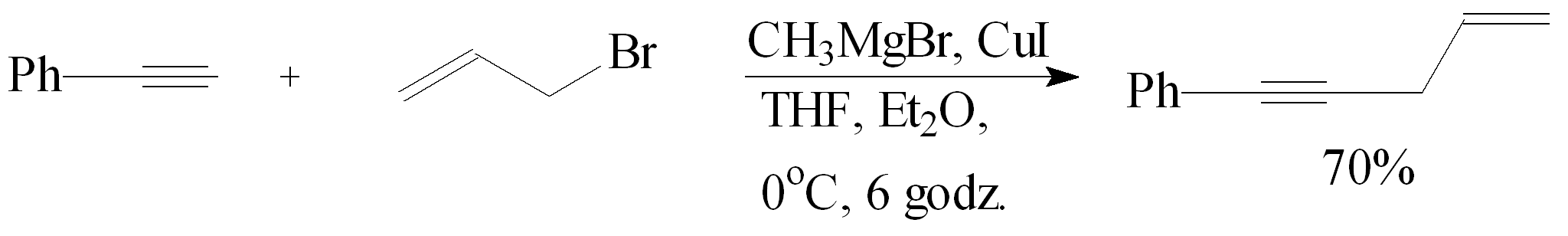
Alami i Ferri40 przeprowadzili reakcje alkilowania fenyloacetylenu bromo i jodoheptynem w pirolidynie w obecności CuI użytego w ilości katalitycznej w temp. 20°C. W reakcji z bromozwiązkiem wykorzystano dodatkowo PdCl2[P(Ph)3]2 jako kokatalizator. Otrzymano 1-fenylonona-1,3-diyn z wydajnością 66-95%.

W kolejnej pracy41 opisano reakcję fenyloacetylenu z 5-jodo-3,3-dimetylopent-1-enem w obecności n-butylolitu. W THF rozpuszczono fenyloacetylen i dodano n-butylolit w HMPT w temp. -78°C. Temp. mieszaniny samorzutnie wzrosła do 0ºC, po czym roztwór mieszano przez 20 min., ochłodzono do temp. -30°C, a następnie dodawano 1-jodo-3,3-dimetylopent-4-en. Temp. reakcji wzrosła do pokojowej i w takich warunkach mieszano roztwór przez 3 godz. Otrzymano 7-fenylo-3,3-dimetylohepten-6-yn z wydajnością 70%.

Reakcję alkilowania fenyloacetylenu 1-jododekanem i 1-bromopentanem przeprowadzono wobec n-butylolitu w mieszaninie heksanu z THF, a reakcję z bromopentanem dodatkowo wobec NaI. Do schłodzonego do temp. -78°C fenyloacetylenu w THF dodano n-butylolit w heksanie. Mieszaninę ogrzano do temp. pokojowej i dodano halogenoalkan oraz, w przypadku 1-bromopentanu, NaI. Reakcję mieszano i ogrzewno do wrzenia przez 12-16 godz. Wydajność 1-fenylododekynu wynosiła 99% a 1-fenyloheptynu, 86%.42
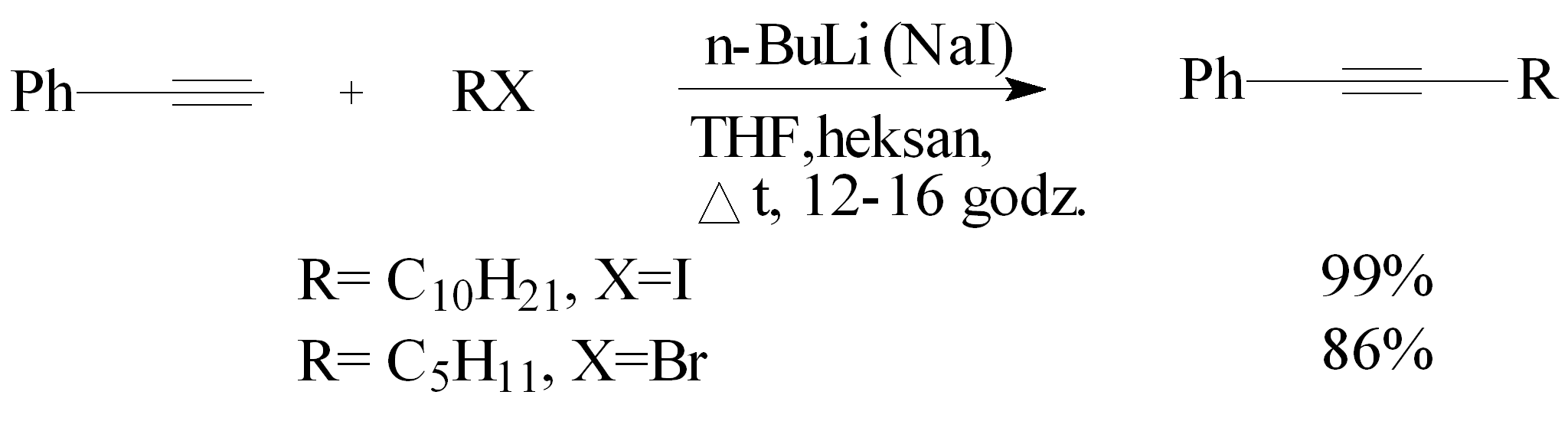
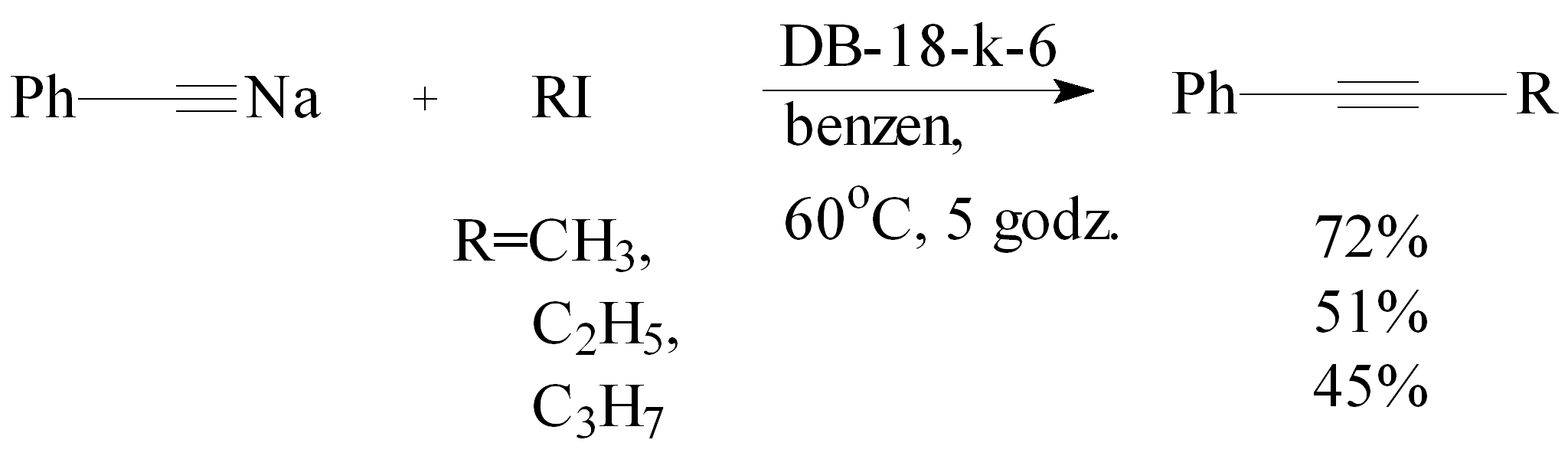
Opisano alkilowanie fenyloacetylenu jodkami alkilowymi w benzenie. Czynnikiem kondensującym był Na zaś katalizatorem eter dibenzo-18-korona-6 (DB-18-k-6). W benzenie rozpuszczono fenyloacetylen oraz dodano Na, a następnie ogrzewano mieszaninę w temp. 60°C przez 1 godz., aż do pełnego przereagowania fenyloacetylenu. Po ochłodzeniu mieszaniny do temp. pokojowej, dodano jodoalkan oraz eter koronowy i reakcję mieszano w temp. 60°C przez 5 godz. Otrzymano produkty alkilowania fenyloacetylenu z wydajnościami 45-72%.43
Autorzy artykułu przeprowadzili te same reakcje bez katalizatora. Nie otrzymano produktów z jodoetanem i propanem zaś z jodometanem wydajność reakcji wynosiła 56%.
Reakcje alkilowania fenyloacetylenu w warunkach PTC
Opisano reakcję alkilowania fenyloacetylenu w obecności stałego KOH oraz eteru 18-korona-6 (18-k-6) w benzenie. Czynnikami alkilującymi były jodometan, jodoetan i 1-jodooktan, a reakcję prowadzono w temp. 80°C przez 1 godz. Otrzymano produkty z wydajnościami 63-74%.44
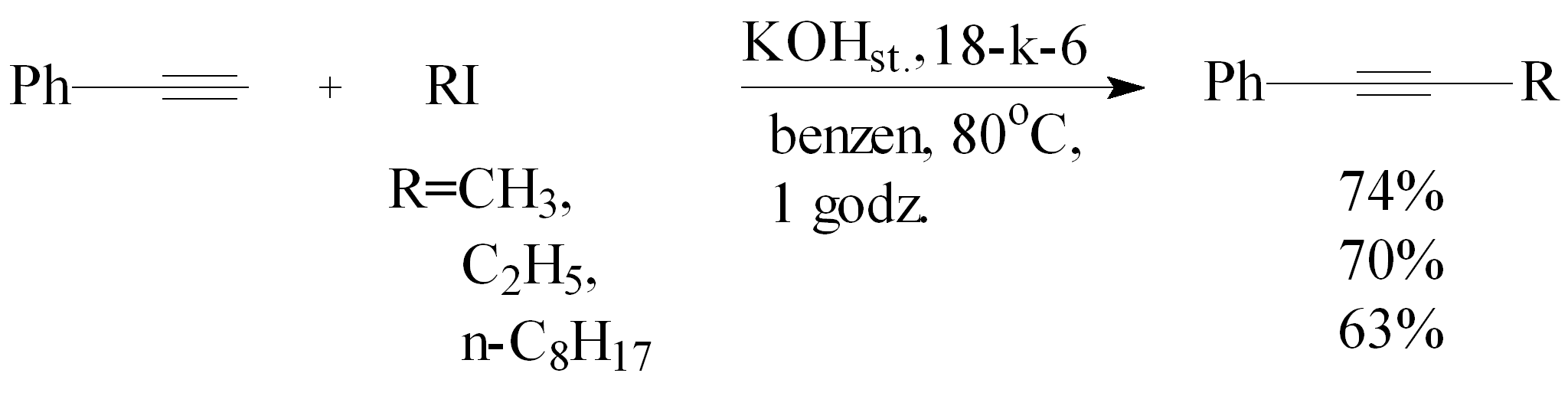
Przeprowadzono alkilowanie fenyloacetylenu w warunkach PTC halogenkami allilowymi w obecności K2CO3, CuI i chlorku tetra-n-butyloamoniowego (TBAC) jako katalizatorów w DMF, w atmosferze gazu obojętnego. Reakcje intensywnie mieszano w temp. 40°C przez 2-4 godz. Wydajności produktów wynosiły 75-90%.45
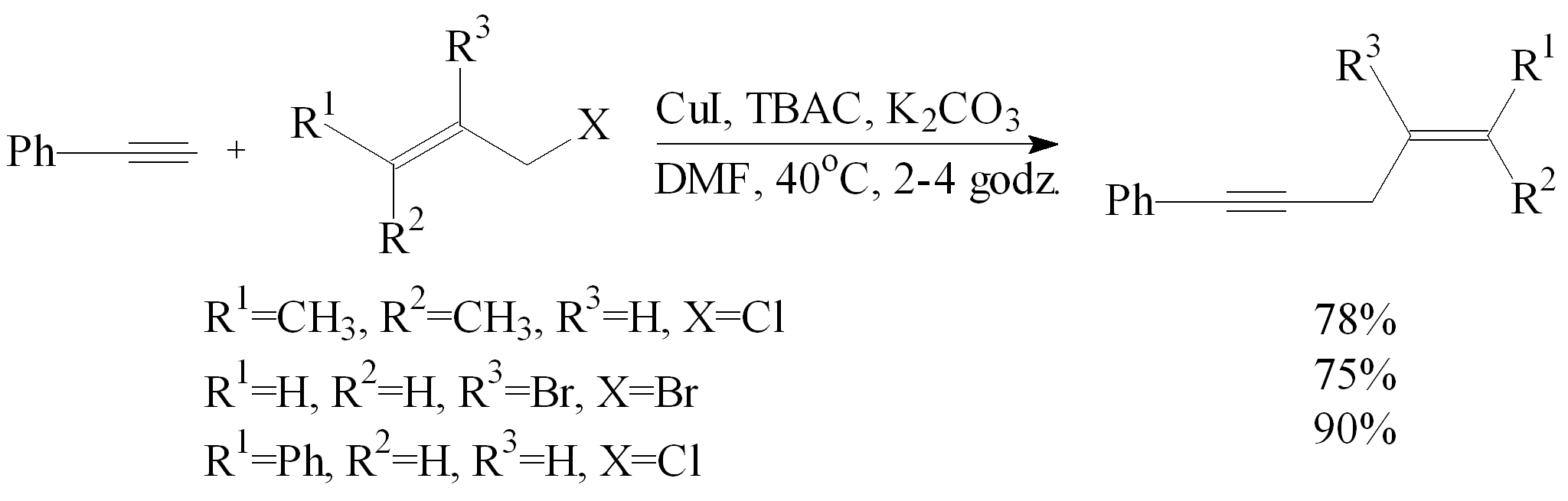
Opisano alkilowanie fenyloacetylenu bromkiem allilu i 3,3-dimetyloallilu wobec 30-50% aq. roztworu NaOH, CuCl oraz TEBA w CH2Cl2. Reakcję prowadzono w atmosferze azotu w temp. 20°C przez 21-23 godz. otrzymując produkty z wydajnościami 89-90%.46

Ponadto autorzy przedstawili możliwy mechanizm powyższych reakcji.
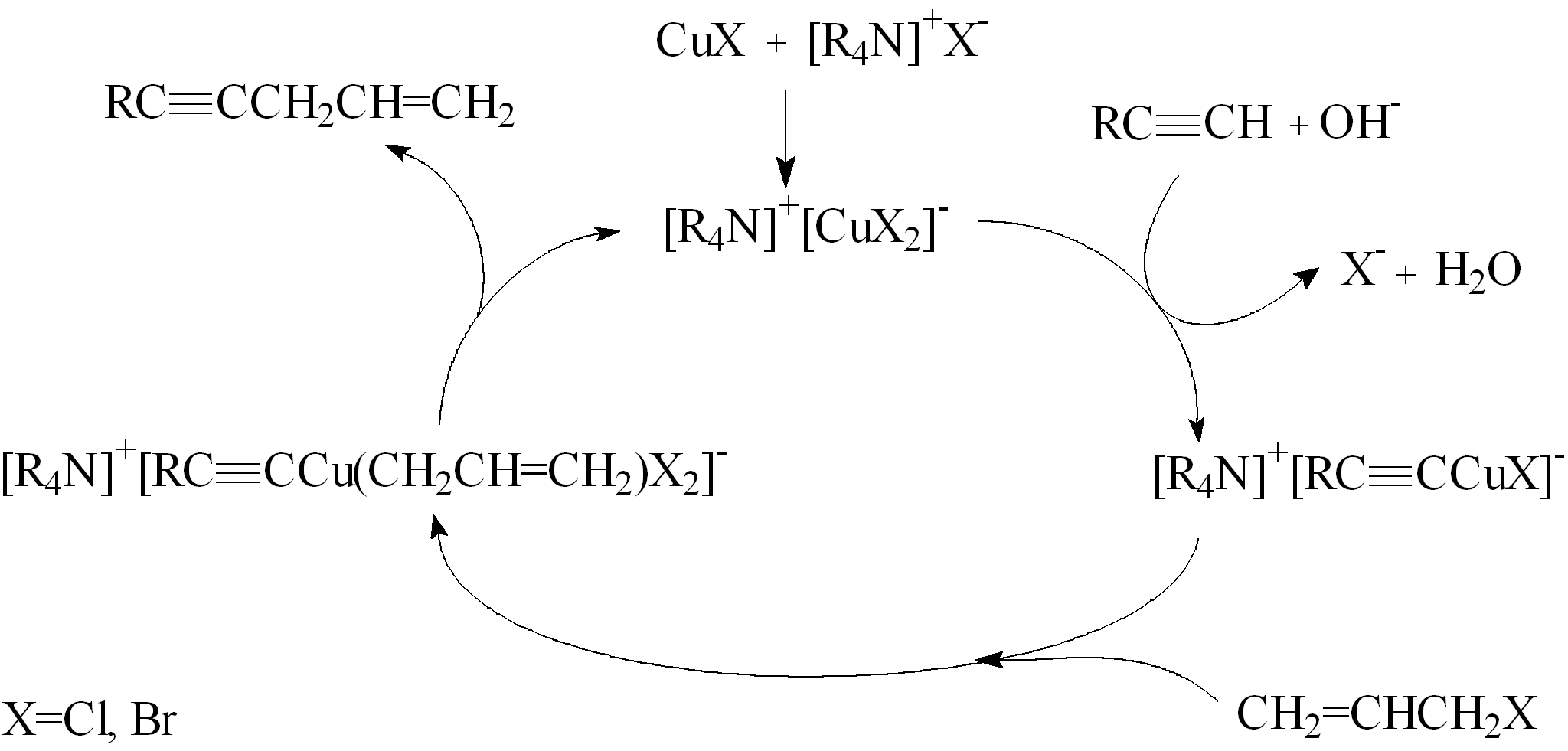
Przeprowadzono reakcję alkilowania fenyloacetylenu 1-bromopropanem w obecności stałego KOH oraz katalizatora przeniesienia międzyfazowego w toluenie. Badano wpływ ilości KOH i rodzaju katalizatora na wydajność procesu. Otrzymano 1-fenylopent-1-yn z wydajnościami 33-87%47 (Tabela 6).

Tabela 6a
| KOH (mmol) | Katalizator | Temp. [°C] | Czas [godz.] | Wydajność [%] | |
| Rodzaj | (mmol) | ||||
| 20 | 18-k-6 | 0,2 | 85 | 4 | 33 |
| 40 | 18-k-6 | 0,2 | 70 | 4 | 66 |
| 40 | 18-k-6 | 0,2 | 110 | 4 | 71 |
| 40 | N+(C8H17)4Brˉ | 0,2 | 80 | 4 | 58 |
| 60 | PEG 1000b | 1,0 | 80 | 4 | 60 |
| 60 | 18-k-6 | 0,2 | 80 | 3 | 82 |
| 60 | 18-k-6 | 0,4 | 80 | 3 | 87 |
| 40 + Cs2CO3c | 18-k-6 | 0,2 | 70 | 4 | 73 |
| 40 + DMSOd | 18-k-6 | 0,2 | 80 | 4 | 81 |
a) warunki reakcji: fenyloacetylen (10 mmol), 1-bromopropan (20 mmol), toluen (5 ml)
b) PEG 1000 – glikolpolietylenowy o masie cząsteczkowej 1000 g/mol
c) dodano równomolowo
d) dodano 1 ml
W 2001 roku opisano alkilowanie fenyloacetylenu 1-bromopentanem w obecności n-butylolitu i jodku tetrabutyloamonowego (TBAI) w THF. Reakcję mieszano w temp. wrzenia rozpuszczalnika. Otrzymano 1-fenylohept-1-yn z wydajnością 90%.42
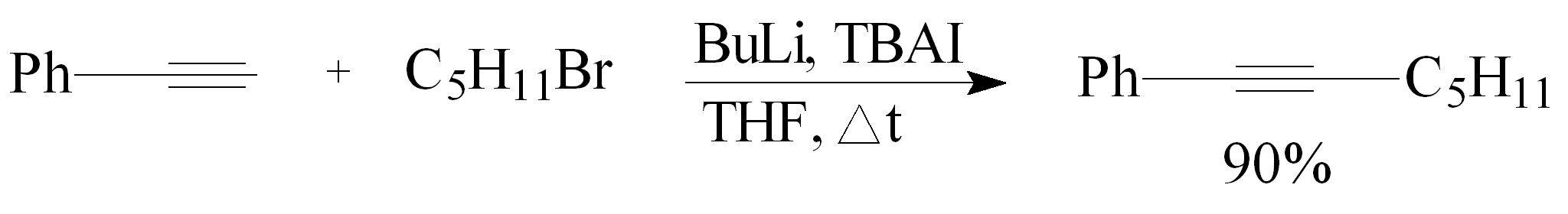
komentarze
Copyright © 2008-2010 EPrace oraz autorzy prac.