
Cykloalkilowanie fenyloacetonitrylu
W oparciu o dane literaturowe21,22 postanowiłem przeprowadzić reakcje cykloalkilowania FAN wobec CsOH w benzenie a jako katalizator użyć TBAB w ilości 5% molowych w stosunku do fenyloacetonitrylu. Zamierzałem nie tylko sprawdzić możliwość zastosowania CsOH w warunkach PTC, chciałem także przekonać się czy użycie tak mocnej zasady pozwoli na wydajne alkilowanie FAN dihaloalkanami. Oczekiwałem, że reakcja będzie przebiegała według następującego równania:
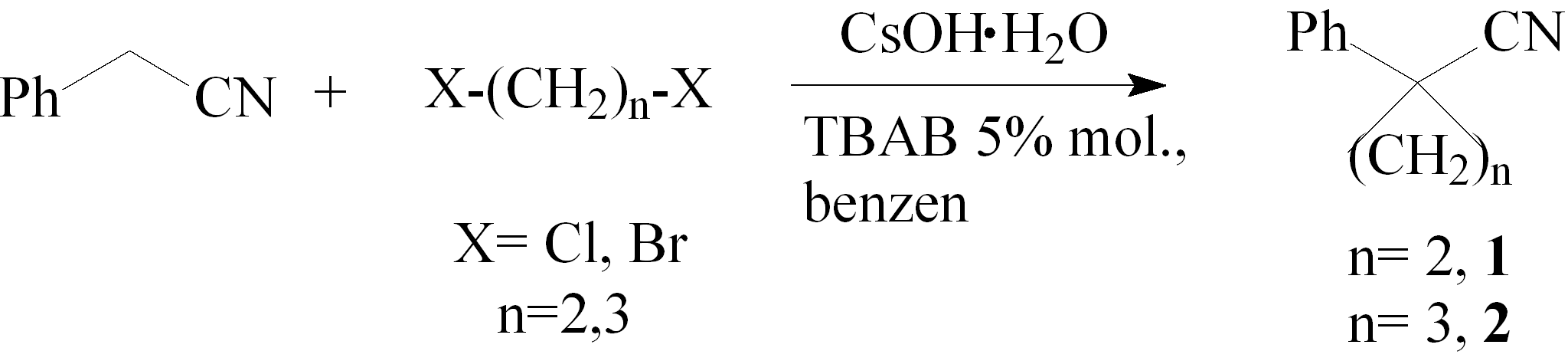
Reakcja fenyloacetonitrylu z 1,2-dichloroetanem
Próby otrzymania 1-cyjano-1-fenylocyklopropanu (1) rozpocząłem od sprawdzenia możliwości użycia 1,2-dichloroetanu. Reagenty oraz zasadę użyłem w następującym stosunku molowym: FAN/ 1,2-dichloroetan/ CsOH·H2O - 1:1.05:4. Jako katalizator użyłem TBAB w ilości 5% molowych w stosunku do FAN. Reakcję przeprowadziłem w temp. pokojowej, a jej przebieg kontrolowałem przez analizę pobieranych próbek metodą chromatografii gazowej (GC). Ponieważ po 6 godz. mieszania w temp. pokojowej nie pojawiły się inne sygnały niż substratów kontynuowałem reakcję w temp. 50°C. Metodą GC stwierdziłem, że w mieszaninie zaczęły pojawiać się nowe związki. Reakcję prowadziłem przez 7 godz.. Kontynuowanie procesu nie prowadziło do wzrostu zawartości produktu w mieszaninie reakcyjnej. Stwierdziłem, że w mieszaninie znajdowało się 25% 1-cyjano-1-fenylocyklopropanu (1), 61% nie przereagowanego FAN, a także trzy związki o czasach retencji: 6.2, 11.3, 14.1 min. Wynik tej reakcji był mało satysfakcjonujący, dlatego przeprowadziłem ją w innych warunkach (Tabela 3).
Tabela 3
| Lp. | Stosunek molowy FAN/ 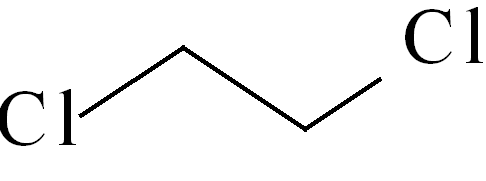 / CsOH·H2O / CsOH·H2O | Temp. [°C] | Czas [godz.] | Skład mieszaniny wg GC [%] | ||
| Produkt 1 | FAN | Inne | ||||
| 1 | 1: 1.05: 4 | tpok. + 50 | 6.0 + 7.0 | 25 | 61 | 14 |
| 2 | 1: 1.05: 5 | 80 | 2.0 | 82 | 13 | 5 |
| 3 | 1: 1.5: 5 | 80 | 4.0 | 98 | 0 | 2 |
| 4a | 1: 1.5:5 | 80 | 3.0 | 87 (61b) | 7 | 4 |
| 5c | 1: 1.5:5 | 80 | 3.0 | 0 | 36 | 64 |
a) reakcja przeprowadzona w powiększonej skali
b) wydajność produktu 1
c) reakcja prowadzona bez katalizatora (TBAB)
Najlepszy wynik osiągnąłem w doświadczeniu Lp. 3 (Tabela 3). Ponieważ próby optymalizacji prowadziłem w bardzo małej skali (2-3 mmole), powtórzyłem reakcję w warunkach optymalnych w większej skali. Wyniki reakcji odbiegały nieco od poprzednich. Po zakończeniu procesu mieszaninę przerobiłem w standardowy sposób a produkt wyizolowałem przez destylację. Otrzymałem 1-cyjano-1-fenylocyklopropan (1) z wydajnością 61% o czystości 96%.
Ponieważ udało mi się otrzymać oczekiwany produkt z dobrą wydajnością spróbowałem przeprowadzić reakcję bez katalizatora przeniesienia międzyfazowego. Użyłem FAN, dichloroetan i CsOH·H2O w stosunku molowym 1:1.2:4. Reakcję prowadziłem w temperaturze wrzenia rozpuszczalnika (80°C) przez 3 godz. Niestety, mieszanina reakcyjna nie zawierała produktu 1.
Reakcja fenyloacetonitrylu z 1,2-dibromoetanem
W przypadku tej reakcji zdecydowałem się na użycie 5-krotnego molowego nadmiaru CsOH·H2O, w celu wyeliminowania niekorzystnego wpływu jonów Brˉ. 1,2-Dibromoetan stosowałem w ilości 1.05 w stosunku do fenyloacetonitrylu, a katalizator TBAB 5% molowych w stosunku do FAN. Reakcję prowadziłem w temp. pokojowej przez 8 godz. W mieszaninie zidentyfikowałem na podstawie GC: 7% FAN, 67% produktu 1 oraz 26% produktów ubocznych (czasy retencji: 9.2, 11.2, 14.1 min.). Spróbowałem uzyskać lepszy wynik zwiększając nadmiar 1,2-dibromoetanu oraz prowadząc reakcję w temp. 80°C. Po upływie 3.25 godz. zawartość cyklopropanu 1 w mieszaninie reakcyjnej wynosiła 96% (wg GC). Powtórzyłem reakcję w większej skali. Po przerobieniu mieszaniny otrzymałem produkt z wydajnością 68% o czystości 88%.
Tak jak w poprzednim doświadczeniu spróbowałem tą samą metodą otrzymać 1-cyjano-1-fenylocyklopropan (1) bez udziału katalizatora. Ku memu zaskoczeniu, w reakcji tej zaczął pojawiać się produkt 1. Po 3 godz. zawartość produktu 1 w mieszaninie reakcyjnej wynosiła 35%. Jednak dalsze prowadzenie reakcji nie zwiększyło tej ilości. W Tabeli 4 zestawiłem warunki przeprowadzonych reakcji.
Tabela 4
| Lp. | Stosunek molowy FAN/ 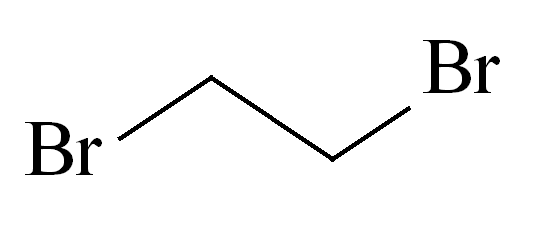 / CsOH·H2O / CsOH·H2O | Temp. [°C] | Czas [godz.] | Skład mieszaniny wg GC [%] | ||
| Produkt 1 | FAN | Inne | ||||
| 1 | 1: 1.05: 5 | tpok | 8.0 | 67 | 7 | 26 |
| 2 | 1: 1.1: 5 | 80 | 3.25 | 96 | 4 | 0 |
| 3a | 1: 1.1: 5 | 80 | 4.0 | 96 (68b) | 2 | 2 |
| 4c | 1: 1.1: 5 | 80 | 3.0 | 35 | 63 | 37 |
a) reakcja przeprowadzona w powiększonej skali
b) wydajność produktu 1
c) reakcja prowadzona bez katalizatora (TBAB)
Reakcja fenyloacetonitrylu z 1,3-dichloropropanem
Tak jak poprzednio nadmiar molowy 1,3-dichloropropanu wynosił 1.05, nadmiar molowy CsOH·H2O był 4-krotny, zaś TBAB użyłem w ilości 5% molowych. Reakcję prowadziłem w temp. 50°C i po upływie 4.25 godz. zawartość 1-cyjano-1-fenylocyklobutanu (2) wynosiła 65%, a nie przereagowanego FAN 6%. W mieszaninie reakcyjnej znajdowały się także produkty uboczne (czasy retencji: 5.4 i 14.2 min.). Następną reakcję prowadziłem w temp. 80°C. Reakcja przebiegała bardzo szybko, ponieważ po 1 godz. zawartość produktu 2 w mieszaninie wynosiła 81%. Zwiększając nadmiar molowy 1,3-dichloropropanu do 1.2 w stosunku do FAN udało mi się zwiększyć stopień przereagowania do 84%. Natomiast prowadząc reakcję w obecności 5-krotnego molowego nadmiaru CsOH·H2O udało mi się zwiększyć ten stopień do 88%. Warunki prowadzenia powyższych reakcji zestawiłem w Tabeli 5.
Tabela 5
| Lp. | Stosunek molowy FAN/  / CsOH·H2O / CsOH·H2O | Temp. [°C] | Czas [godz.] | Skład mieszaniny wg GC [%] | ||
| Produkt 2 | FAN | Inne | ||||
| 1 | 1: 1.05: 4 | 50 | 4.25 | 65 | 6 | 29 |
| 2 | 1: 1.05: 4 | 80 | 1.0 | 81 | 7 | 12 |
| 3 | 1: 1.2: 4 | 80 | 1.0 | 84 | 10 | 6 |
| 4 | 1: 1.2: 5 | 80 | 1.0 | 88 | 2 | 10 |
| 5a | 1: 1.2: 4 | 80 | 1.5 | 90 (65b) | 0 | 10 |
| 6c | 1: 1.2: 4 | 80 | 4.0 | 0 | 0 | 100 |
a) reakcja przeprowadzona w powiększonej skali
b) wydajność produktu 2
c) reakcja prowadzona bez katalizatora (TBAB)
Chociaż w doświadczeniu L.p. 4 zaobserwowałem największy stopień przereagowania substratów, do zbadania wydajności wykorzystałem reakcję z doświadczenia L.p. 3. W tych warunkach zawartość produktu 2 była nieco niższa, ale prowadziłem reakcję z mniejszą ilością zasady.
W Tabeli 5 zamieściłem również wynik reakcji bez użycia katalizatora TBAB. W tym przypadku, tak jak w reakcji FAN z 1,2-dichloroetanem, nie zauważyłem pojawienia się produktu cykloalkilowania.
Reakcja fenyloacetonitrylu z 1,3-dibromopropropanem
Badanie rozpocząłem od przeprowadzenia reakcji w temperaturze pokojowej, używając substraty w stosunku molowym: FAN/ 1,3-dibromopropan/ CsOH·H2O – 1 : 1.05 : 5 i jak zwykle TBAB, 5% molowych w stosunku do FAN. Wynik reakcji po 4 godz. okazał się zaskakująco dobry, bowiem w mieszaninie reakcyjnej znajdowało się aż 92% 1-cyjano-1-fenylocyklobutanu (2), tylko 2% FAN i 6% produktów ubocznych (czasy retencji: 4.4, 5.4, 9.5 min.). W kolejnym wariancie postanowiłem zwiększyć ilość 1,3-dibromopropanu do 1.1 mola względem FAN oraz podwyższyć temp. do 80°C. W takich warunkach już po 45 min. reakcja przebiegła praktycznie ilościowo, a zawartość pochodnej cyklobutanu 2 wynosiła 96%. Wyniki przeprowadzonych reakcji są zbliżone ale czas drugiego doświadczenia jest ponad 4-krotnie krótszy.
Reakcję w tych warunkach powtórzyłem bez katalizatora. Proces trwał 4 godz., a zawartość cyklobutanu 2 w mieszaninie reakcyjnej wynosiła 69%. W Tabeli 6 zestawiłem warunki oraz wyniki przeprowadzonych reakcji.
Tabela 6
| Lp. | Stosunek molowy FAN/  / CsOH·H2O / CsOH·H2O | Temp. [°C] | Czas [godz.] | Skład mieszaniny wg GC [%] | ||
| Produkt 2 | FAN | Inne | ||||
| 1 | 1: 1.05: 5 | tpok. | 4.0 | 92 | 1 | 7 |
| 2 | 1: 1.1: 5 | 80 | 0.75 | 96 | 0 | 4 |
| 3a | 1: 1.1: 5 | 80 | 0.75 | 96 (74b) | 0 | 4 |
| 4c | 1: 1.1: 5 | 80 | 4.0 | 69 | 0 | 31 |
a) reakcja przeprowadzona w powiększonej skali
b) wydajność produktu 2
c) reakcja prowadzona bez katalizatora (TBAB)
komentarze
Copyright © 2008-2010 EPrace oraz autorzy prac.