
Kondensacja Darzens’a chlorooctanu t-butylu ze związkami karbonylowymi
W rozdziale tym opisałem wyniki badań kondensacji Darzens’a chlorooctanu t-butylu z benzaldehydem, acetofenonem, cyklopentanonem i cykloheksanonem. Reakcje prowadziłem w obecności 50% aq. KOH w układzie ciecz-ciecz oraz sproszkowanego KOH i CsOH·H2O w układzie ciało stałe-ciecz, jako katalizator wykorzystałem TBAB w ilości 5% molowych. Reakcje prowadziłem w benzenie w temp. pokojowej. Spodziewałem się, że będą one przebiegać w następujący sposób:
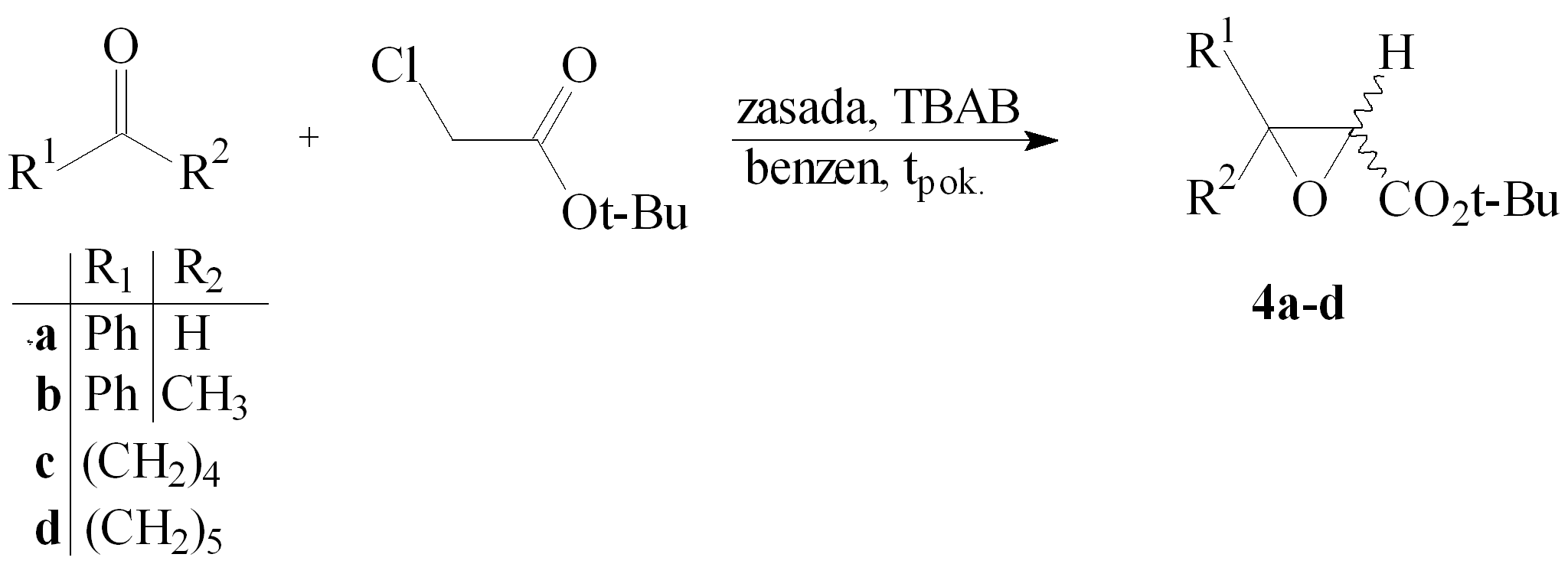
Chlorooctan t-butylu otrzymałem z chlorku chloroacetylu i alkoholu t-butylowego wobec N,N-dimetyloaniliny z wydajnością 52% (wyd. lit.141 60%).
Reakcja chlorooctanu t-butylu z benzaldehydem
Jako pierwszy związek karbonylowy do badań kondensacji Darzens’a użyłem benzaldehyd ponieważ z danych literaturowych wynika, iż łatwo wstępuje on w tę reakcję. Reakcję przeprowadziłem stosując chlorooctan t-butylu w 1.2-krotnym molowym nadmiarze w stosunku do benzaldehydu wobec katalizatora TBAB i sproszkowanego KOH (5-krotny molowy nadmiar), w benzenie w temp. pokojowej do czasu, gdy analiza GC wykazała brak substratów (1.25 godz.). Mieszanina reakcyjna zawierała 71% Z-β-fenylo-α,β-epoksypropionianu t-butylu (Z-4a), 21% E-β-fenylo-α,β-epoksypropionianu t-butylu (E-4a) oraz 8% innych produktów o czasach retencji: 5.3 (4%) i 10.5 (4%) min.
Kolejną reakcję chlorooctanu t-butylu z benzaldehydem przeprowadziłem wobec 50% aq. roztworu KOH (5-krotny molowy nadmiar). Pozostałe reagenty użyłem w takich samych ilościach. Reakcję prowadziłem w benzenie w temp. pokojowej aż do zaniku substratów (3 godz.). Otrzymałem mieszaninę reakcyjną o składzie: 79% produktu Z-4a oraz 16% produktu E-4a, a także jeden produkt uboczny o czasie retencji 10.5 min. w ilości 5%. W Tabeli 7 zestawiłem warunki reakcji oraz uzyskane wyniki.
Tabela 7
| Stosunek molowy benzaldehyd/ chlorooctan t-butylu/ zasada | Zasada | Temp. [°C] | Czas [godz.] | Skład mieszaniny wg GC [%] | |
| Produkty 4a | Inne | ||||
| 1: 1.2: 5 | KOHst. | tpok. | 1.25 | Z-72 E-21 | 8 |
| 1: 1.2: 5 | 50%aq.KOH | tpok. | 3.0 | Z-79 E-16 | 5 |
Reakcja chlorooctanu t-butylu z acetofenonem
Jako kolejny związek karbonylowy do badań nad kondensacją Darzens’a wykorzystałem acetofenon. Pierwszą reakcję przeprowadziłem przy użyciu stałego KOH i katalizatora TBAB w benzenie. Reagenty były użyte w następującym stosunku molowym: acetofenon, chlorooctan t-butylu, KOH, kat. TBAB – 1: 1.2 : 5 : 0.05. Reakcję prowadziłem w temp. pokojowej i po 1 godz. analiza GC wykazała, że zaczęły pojawiać się produkty w ilości 36%. Po porównaniu ze wzorcem zidentyfikowałem je jako izomery Z (24%) i E (12%) β-fenylo-β-metylo-α,β-epoksypropionianu t-butylu (4b), ponadto w mieszaninie znajdowało się 10% chlorooctanu t-butylu, 31% acetofenonu oraz 23% innych związków. Postanowiłem reakcję prowadzić przez następne 3 godz.. Metodą GC stwierdziłem, że po tym czasie mieszanina zawierała 28% izomeru Z-4b, 12% izomeru E-4b, 30% acetofenonu oraz 30% 18 związków w niewielkich ilościach.
W kolejnym wariancie reakcję przeprowadziłem w dokładnie takich samych warunkach i z takimi samymi ilościami reagentów, a jedynie postanowiłem użyć 50% aq. roztwór KOH w 5-krotnym molowym nadmiarze względem acetofenonu. Reakcję prowadziłem w benzenie w temp. pokojowej przez 9.5 godz. Stwierdziłem, że mieszanina zawierała jedynie 3% izomeru Z-4b oraz 2% izomeru E-4b oraz: chlorooctan t-butylu (5%), acetofenon (80%) oraz inne 2 związki w ilości 10% [czasy retencji: 8.9 (4%), 11.1 (6%) min.].
W reakcji tej postanowiłem użyć mocniejszej zasady jaką jest CsOH·H2O w 5-krotnym molowym nadmiarze. Pozostałe reagenty zostały użyte w takiej samej ilości jak poprzednio. Reakcję przeprowadziłem w benzenie w temp. pokojowej i przerwałem ją gdy analiza GC wykazała brak chlorooctanu t-butylu (2.5 godz.). Mieszanina reakcyjna zawierała 23% acetofenonu, 47% izomeru Z-4b oraz 24% izomeru E-4b oraz 3 związki o czasach retencji: 6.5 (1%), 8.9 (1%), 11.1 (4%) min. Był to najlepszy wynik kondensacji Darzens’a chlorooctanu t-butylu z acetofenonem. W Tabeli 8 zestawiłem wyniki oraz warunki reakcji.
Tabela 8
| Stosunek molowy acetofenon/ chlorooctan t-butylu/ zasada | Zasada | Temp. [°C] | Czas [godz.] | Skład mieszaniny wg GC [%] | ||
| Produkty 4b | Acetofenon | Inne | ||||
| 1 : 1.2 : 5 | KOHst. | tpok. | 3.0 | Z-28 E-12 | 30 | 30 |
| 1 : 1.2 : 5 | 50%aq.KOH | tpok. | 9.5 | Z-3 E-2 | 80 | 10 |
| 1 : 1.2 : 5 | CsOH·H2O | tpok. | 2.5 | Z-47 E-24 | 23 | 6 |
Reakcja chlorooctanu t-butylu z cyklopentanonem
Kolejno przeprowadziłem kondensację Darzens’a cyklopentanonu i chlorooctanu t-butylu (1.2 mola) wobec sproszkowanego KOH (5-krotny molowy nadmiar) oraz TBAB (5% molowych). Reakcję prowadziłem w benzenie w temp. pokojowej prze z 7.5 godz. Po tym czasie analiza GC wykazała w mieszaninie reakcyjnej 77% cyklopentanonu oraz 2 związki o czasach retencji: 8.3 (12%), 11.4 (11%) min. Niestety nie posiadałem wzorca estru t-butylowego kwasu 1-oksospiro[2.4]heptano-2-karboksylowego (4c), a małe ilości otrzymanych w reakcji związków nie pozwalały na ich wydzielenie i identyfikację. Mogę jedynie przypuszczać, że związek o czasie retencji 8.3 jest estrem t-butylowym kwasu 1-oksospiro[2.4]heptano-2-karboksylowego (4c).
Tę samą reakcje przeprowadziłem z wykorzystaniem 4-krotnego molowego nadmiaru CsOH·H2O względem cyklopentanonu (pozostałe warunki bez zmian) w benzenie w temp. pokojowej. Po upływie 1.5 godz. w mieszaninie znajdowało się 65% cyklopentanonu oraz 35% niezidentyfikowanych związków o czasach retencji: 8.3 (16%), 8.9 (6%), 11.1 (2%), 11.6 (8%), 11.9 (2%), 12.7 (1%) min. Wyniki reakcji zestawiłem w Tabeli 9.
Tabela 9
| Stosunek molowy cyklopentanon/ chlorooctan t-butylu/ zasada | Zasada | Temp. [°C] | Czas [godz.] | Nieprzereagowany cyklopentanon [%] | Produkty | |
| Czasy retencji [min.] | Zawartość w mieszaninie [%] | |||||
| 1 : 1.2 : 5 | KOHst. | tpok. | 7.5 | 77 | 8.3 11.4 | 12 11 |
| 1 : 1.2 : 4 | CsOH·H2O | tpok. | 1.5 | 65 | 8.3 8.9 11.1 11.6 11.9 12.7 | 16 6 2 8 2 1 |
Reakcja chlorooctanu t-butylu z cykloheksanonem
Badałem także kondensację chlorooctanu t-butylu z cykloheksanonem. Badanie rozpocząłem używając reagenty w następującym stosunku molowym: stały KOH - 5-krotny nadmiar, TBAB – 5%, chlorooctan t-butylu - 1.1-krotny nadmiar oraz cykloheksanon – równoważnik. Reakcję prowadziłem w benzenie w temp. pokojowej kontrolując jej przebieg metodą GC. Po upływie 5.5 godz. w mieszaninie znajdowało się 35% chlorooctanu t-butylu, 40% cykloheksanonu, 23% związku o czasie retencji 9.1 min. oraz 2% związku o czasie retencji 11.1 min. Kontynuowałem reakcję przez 13 godz. i wtedy analiza GC wykazała obecność chlorooctanu t-butylu (2%), cykloheksanonu (57%) oraz 2 wyżej wymienionych związków w ilościach 34% (9.1 min.) i 4% (11.1 min.) a także związek o czasie retencji 8.9 min. w ilości 3%. Ze względu na skalę, w jakiej prowadziłem reakcję (~2 mmol) oraz niski stopień przereagowania nie mogłem oczyścić mieszaniny i zidentyfikować produktów.
Kolejną reakcję przeprowadziłem przy użyciu 50% aq. roztworu KOH użytym (5-krotnym molowym nadmiarze), pozostałe reagenty jak poprzednio. Reakcję prowadziłem w benzenie w temp. pokojowej przez 7 godz. Wyniki analizy GC wykazały, iż mieszanina reakcyjna zawierała 91% cykloheksanonu, 7% związku o czasie retencji 9.1 min. oraz 2% związku o czasie retencji 9.6 min.
W następnym doświadczeniu wykorzystałem CsOH·H2O (4-krotny molowy nadmiar), chlorooctan t-butylu (1.2-krotny molowy nadmiar) oraz 5% molowych TBAB. Reakcję prowadziłem w benzenie w temp. pokojowej kontrolując jej przebieg metodą GC. Już po upływie 1 godz. mieszanina reakcyjna zawierała 3 produkty pojawiające się we wcześniejszych doświadczeniach, były to związki o czasach retencji: 8.9 (2%), 9.1 (59%), 11.1 (16%) min. oraz 2% chlorooctanu t-butylu, 15% cykloheksanonu, a także 11 związków w niewielkich ilościach. Reakcję jednak kontynuowałem dalej i zakończyłem ją po 3 godz. Analiza wykazała, że mieszanina zawierała 14% cykloheksanonu oraz produkty o czasach retencji: 8.9 (4%), 9.1 (61%), 9.6 (1%), 11.1 (17%), 12.1 (2%), 12.4 (1%) min..
Wynik tej reakcji nie wydawał się zadowalający, dlatego postanowiłem ją powtórzyć zwiększając nadmiar CsOH·H2O do 5-krotnego molowego (pozostałe warunki reakcji bez zmian). Po upływie 3 godz. przerwałem reakcję i zbadałem próbkę mieszaniny metodą GC. Analiza wykazała, że w mieszaninie reakcyjnej znajdowało się 25% cykloheksanonu oraz 3 związki o czasach retencji: 9.1 (68%), 9.6 (2%) 11.1 (5%) min.
Wynik tej reakcji był na tyle dobry, że postanowiłem ją powtórzyć w większej skali (~10 mmol). Reakcję prowadziłem przez 2 godz. (do zaniku chlorooctanu t-butylu). Mieszanina reakcyjna zawierała 28% cykloheksanonu, a także 4 związki o czasach retencji: 9.1 (60%), 11.1 (8%), 12.1 (2%), 12.4 (2%) min. Po zakończeniu procesu mieszaninę reakcyjną rozcieńczyłem wodą, przerobiłem w standardowy sposób a produkt o czasie retencji 9.1 wyizolowałem przez destylację. Otrzymałem go z wydajnością 43% o czystości 82%. Niska czystość produktu spowodowana była obecnością 18% związku o czasie retencji 11.1 min. Destylat poddałem więc rozdziałowi na kolumnie chromatograficznej wypełnionej żelem krzemionkowym (eluent: heksan nasycony MeOH). Udało mi się uzyskać produkt o czystości 87% w 13% zanieczyszczony związkiem o czasie retencji 11.1 min. i w takiej postaci poddałem go identyfikacji za pomocą widma 1H NMR.
Wyniki przeprowadzonych reakcji zebrałem w Tabeli 10.
Tabela 10
| Stosunek molowy cykloheksanon/ chlorooctan t-butylu/ zasada | Zasada | Temp. [°C] | Czas [godz.] | Nieprzereagowany cykloheksanon [%] | Produkty | |
| Czasy retencji [min.] | Zawartość w mieszaninie [%] | |||||
| 1 : 1.1 : 5 | KOHst. | tpok. | 13 | 57 | 8.9 9.1 11.1 | 3 34 4 |
| 1 : 1.1 : 5 | 50%aq.KOH | tpok. | 7 | 91 | 9.1 9.6 | 7 2 |
| 1 : 1.2 : 4 | CsOH·H2O | tpok. | 3 | 14 | 8.9 9.1 9.6 11.1 12.1 12.4 | 4 61 1 17 2 1 |
| 1 : 1.2 : 5 | CsOH·H2O | tpok. | 3 | 25 | 9.1 9.6 11.1 | 68 2 5 |
| 1 : 1.2 : 5a | CsOH·H2O | tpok. | 2 | 28 | 9.1 11.1 12.1 12.4 | 60 (43)b 8 2 2 |
a) reakcja przeprowadzona w powiększonej skali
b) wydajność produktu o czasie retencji 9.1 o czystości 87%
Wyniki widma H1NMR:
H1NMR (CDCl3), δ[ppm]: 1.41 (s, 9H, t-C4H9), 1.40-1.76 (m, 10H, c-C6H10), 3.14 (s, 1H, CH).
Z analizy widma wynika, iż jest to ester t-butylowy kwasu 1-oksospiro[2.5]oktano-2-karboksylowego (4d).
Reakcja chlorooctanu t-butylu w warunkach PTC
Ponieważ w większości reakcji, które przeprowadziłem pojawiał się związek o czasie retencji 11.1 min., podejrzewałem, że jest to produkt kondensacji jednego z reagentów. Postanowiłem więc przeprowadzić reakcję chlorooctanu t-butylu w warunkach PTC. Użyłem sproszkowany KOH w 5-krotnym molowym nadmiarze oraz TBAB w ilości 5% molowych. Reakcję prowadziłem w benzenie w temp. pokojowej kontrolując jej przebieg metodą GC. Po upływie 3 godz. mieszanina reakcyjna zawierała trzy związki o czasach retencji: 7.8 (35%), 8.9 (32%), 11.1 (33%) min. i nie zawierała chlorooctanu t-butylu. Pomimo tego prowadziłem reakcję dalej i po upływie 5 godz. stwierdziłem obecność tylko produktu o czasie retencji 11.1 min. Po standardowym przerobieniu mieszaniny otrzymałem produkt w postaci mętnego oleju, z którego po rozpuszczeniu w metanolu wykrystalizował produkt o czystości 92%. Związek ten poddałem identyfikacji za pomocą widma 1H NMR.
H1NMR (CDCl3), δ[ppm]: 1.45 (s, 9H, t-C4H9), 1.45 (s, 18H, 2·t-C4H9), 2.36 (d, JCD=5.2 Hz, 2H, 2·CHC), 2.58 (t, JDC= 5.6 Hz, 1H, CHD)
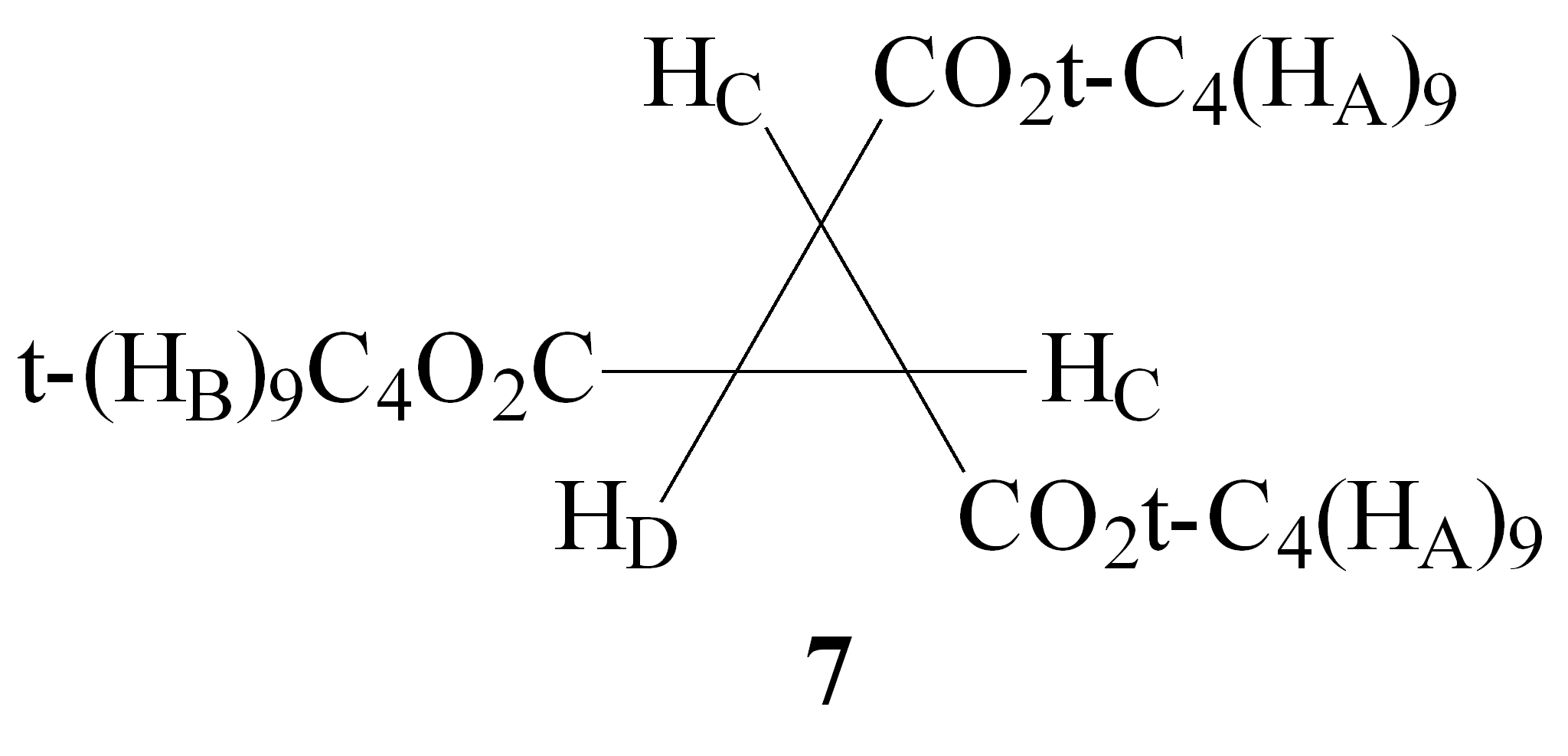
Z danych spektralnych wynika, iż jest to ester t-butylowy kwasu trans-cyklopropano-1,2,3-trikarboksylowego (7), który powstaje najprawdopodobniej następującą drogą:
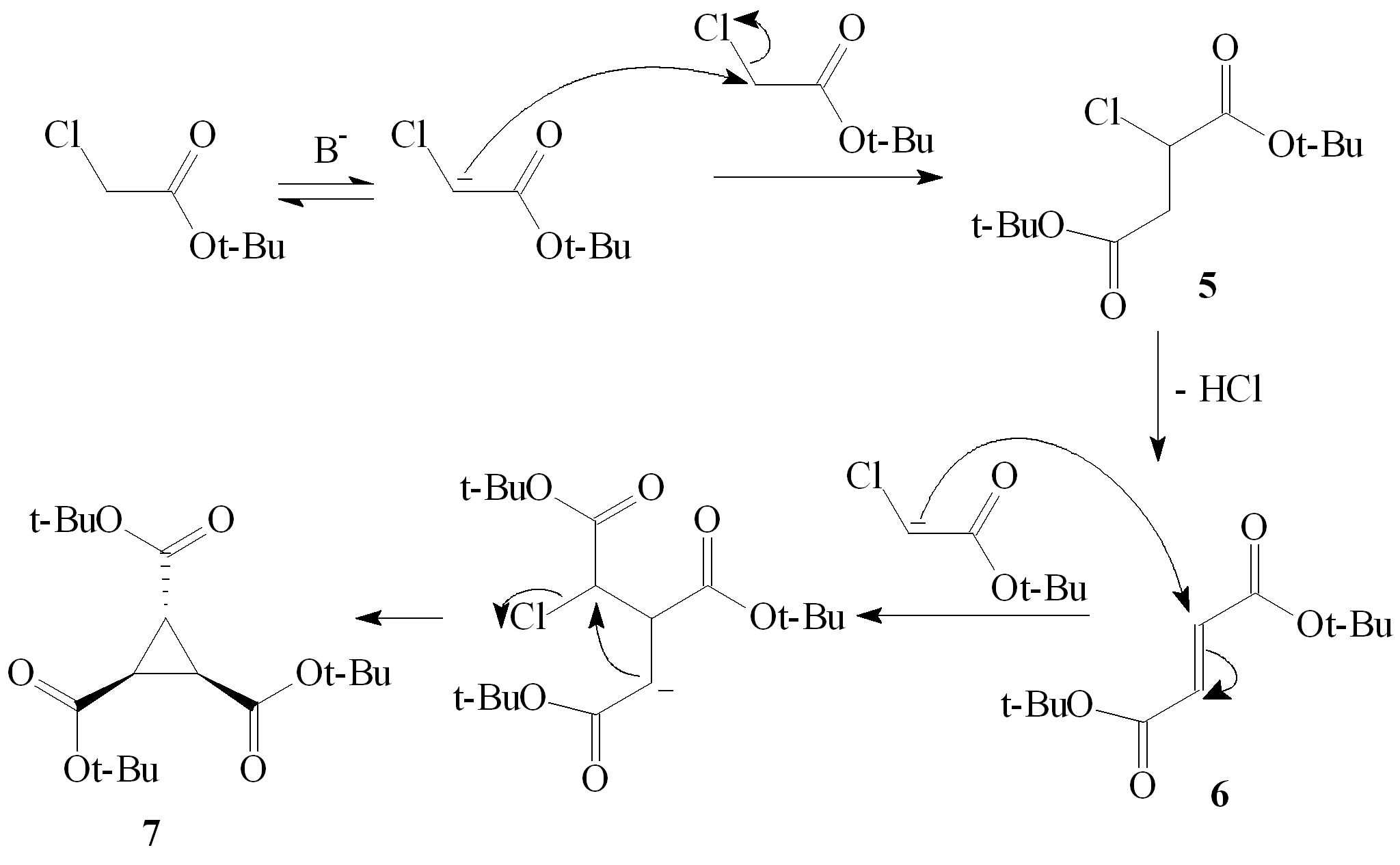
Powstające w trakcie reakcji związki o czasach retencji: 7.8 i 8.9 min. to przypuszczalnie związki 5 i 6.
komentarze
Copyright © 2008-2010 EPrace oraz autorzy prac.